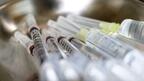
Предлагат облекчени правила за изпитания на лекарства в ЕС
Директивата за клиничните изследвания намали броя им с 25% за пет години
Клиничните изпитания на лекарствата са от първостепенно значение за разработването на нови медикаменти и начини за лечение. В ЕС действа специална директива по отношение на клиничните изпитания, която беше разработена през 2001 година.
Ревизиите на документа показаха, че тя осигурява високо равнище на безопасност на пациентите, но в същото време различията при нейното транспониране в националното законодателство ограничават нейното действие. Така в периода 2007 – 2011 година клиничните изпитания на лекарствата са с 25% по-малко.
По тази причина от ЕК предлагат замяната на директивата с регламент. В текстовете му са записани ускорени и облекчени процедури, които обаче ще осигурят по-голяма прозрачност при изпитанията както в ЕС, така и в трети държави.
Конкретните предложения включват процедура за разрешение на клинични изпитания, която да даде възможност за задълбочен анализ на заявлението. Освен това процедурите за докладване на резултатите ще бъдат опростени – така ще бъде спестено задължението на изследователите да представят поотделно на различните органи и държави в ЕС информацията за клиничното изследване.
Изследователите ще трябва да дават и повече информация относно участниците в изпитанията и резултатите от тях.
Коментари
ТВ програма
Кино
- Сега Бързо, лесно, вкусно
- 16:30 Светът и ние
- 16:55 България в 60 минути с Мариана...
- 18:00 По света и у нас
- 18:30 Още от деня коментарно предаване
- 19:00 Последният печели...
- 20:00 По света и у нас
- 20:45 Спортни новини
- Сега Премиера: "Моите братя и сестри" -...
- 17:00 bTV Новините
- 17:20 "Лице в лице" - публицистично...
- 18:00 "Стани богат" - телевизионна игра с...
- 19:00 bTV Новините - централна емисия
- 20:00 "Островът на 100-те гривни: Другата...
- 23:00 bTV Новините - късна емисия
- 23:30 "В ръкавиците на Пулеви" - спортна...
- Сега "Пресечна точка" - публицистично шоу
- 17:00 "Семейни войни" - телевизионна игра
- 18:00 "Сделка или не" (премиера) -...
- 19:00 Новините на NOVA - централна емисия
- 20:00 "Игри на волята:...
- 22:00 "Big Brother" (премиера) - риалити,...
- 23:00 Новините на NOVA
- 23:30 "ФБР" - сериал, сезон 1